СТВОЛОВЫЕ КЛЕТКИ МОБИЛИЗОВАННЫЕ ИЗ ПЕРИФЕРИЧЕСКОЙ КРОВИ
Возраст связан как с гематологическими, так и с негематологическими нарушениями. ГСК – незрелые клетки, которые могут развиваться во все типы клеток крови. Отношения между ГСК и поддерживающими их нишевыми клетками функционально нарушены в старости.
Но, старческая система кроветворения может быть восстановлена за счет молодой мобилизованной периферической крови, ГСК . МикроРНК в секретируемых микровезикулах ответственны за улучшение гемопоэтических функций за счет увеличения экспрессии генов, нацеленных на MYC и E2F, и снижения экспрессии p53.
При восстановлении наблюдалось увеличение количества NK-киллеров, что могло устранить стареющие клетки по мере их появления в различных органах.
Восстановленные клетки могут также помочь в регенерации состарившихся гемопоэтических и негематопоэтических поддерживающих клеток микросреды костного мозга.
www.journals.plos.org/plosbiology/article?id=10.1371/journal.pbio.0050201www.aging-us.com/article/203689/text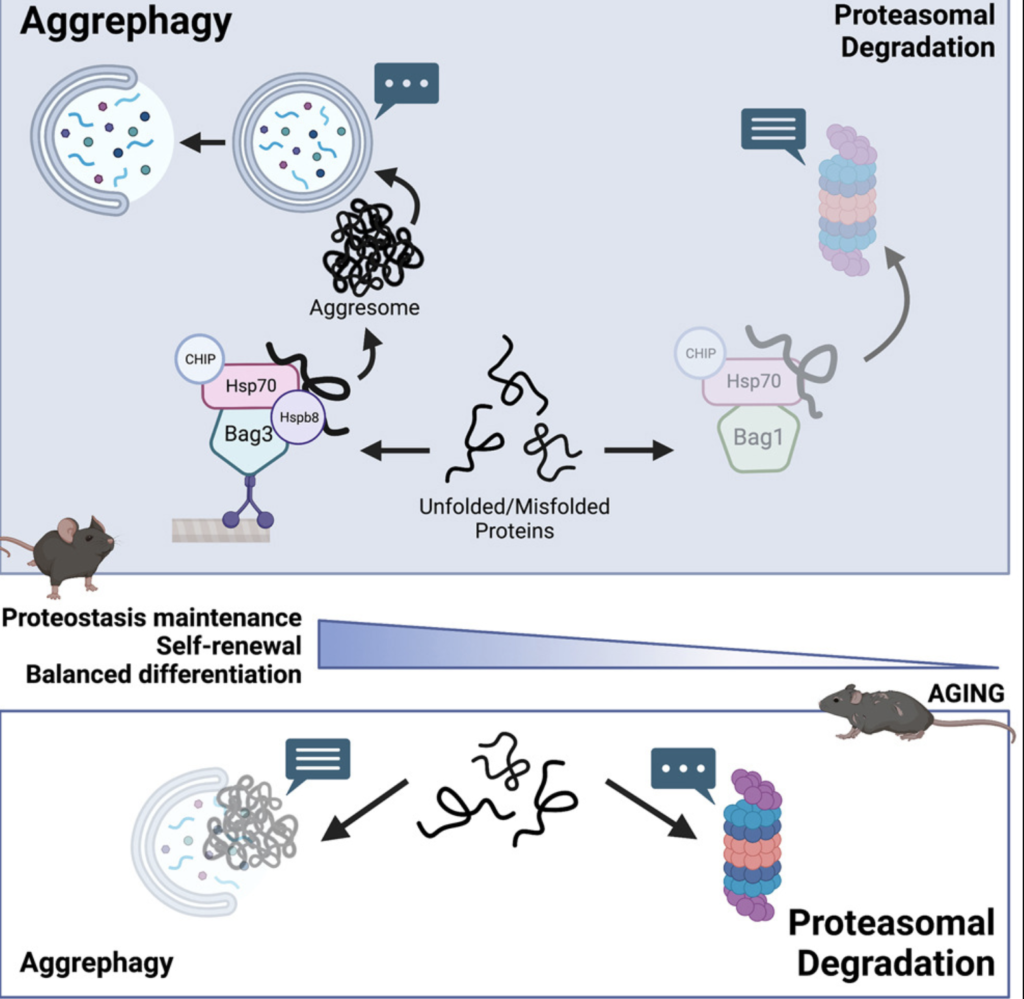
Мы (CIRM) разработали и с 2006 года успешно используем технологию предполагающую трансплантацию аутологичных гемопоэтических (мезенхимальных) стволовых клеток в более старшем возрасте. ГСК мобилизованные в молодом возрасте и вводимые в организм по определенной программе в старшем возрасте помимо иммунной перезагрузки организма, а в случае применения генной терапии EX VIVO восстановления поликлональности, обладают дополнительными свойствами.
Гемопоэтические стволовые клетки (ГСК) регенерируют клетки крови и иммунитета на протяжении всей жизни. Старение HSC связано с тяжелой потерей агресом и снижением аутофагического потока. Пути деградации белка, таким образом, специфически настроены в молодых взрослых HSC для сохранения протеостаза и приспособленности, но становятся нерегулируемыми во время старения. ГСК, синтезируют белки гораздо медленнее, чем другие типы клеток, отдавая предпочтение качеству, а не количеству. Это помогает им совершать меньше ошибок в процессе, так как неправильно свернутые белки могут стать токсичными для клеток, если им позволить накапливаться. Тем не менее, некоторые ошибки или повреждение белков неизбежны, но стволовые клетки обеспечивают правильное удаление этих белков.
В отличие от большинства клеток, которые используют протеасомы для деградации неправильно свернутых белков, HSCs переносят неправильно свернутые белки в агресомы Bag3-зависимым образом и зависят от агрефагии, селективной формы аутофагии, для поддержания протеостаза in vivo. Когда аутофагия отключена, ГСК компенсируют это увеличением активности протеасом, но протеостаз в конечном итоге нарушается по мере накопления белковых агрегатов и нарушения функции ГСК. Дефицит притупляет образование агресом в HSCs, что приводит к накоплению белковых агрегатов, миелоидной дифференцировке и снижению активности самообновления. Пути деградации белка, таким образом, специфически настроены в молодых взрослых HSC для сохранения протеостаза и приспособленности, но становятся нерегулируемыми во время старения приводя к раку, диабету, возраст-зависимым болезням. www.sciencedirect.com/…/pii/S1934590923000711…

