ЭПИГЕНЕТИКА
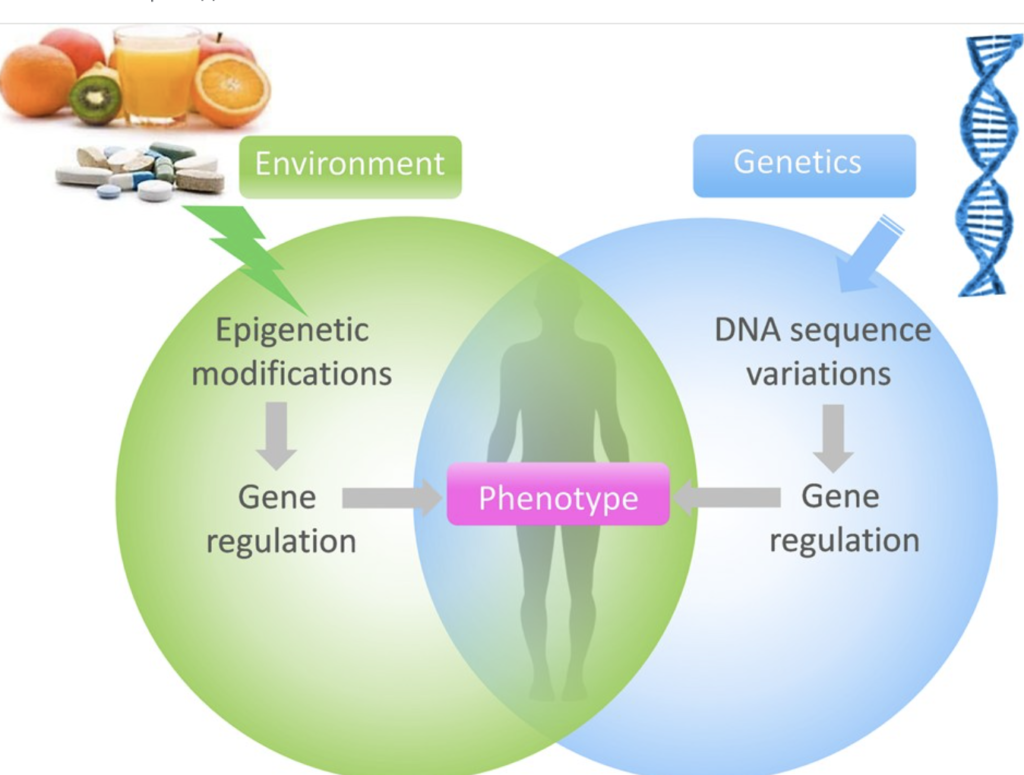
Ваше поведение и окружающая среда могут привести к изменениям, влияющим на работу ваших генов. В отличие от генетических изменений, эпигенетические изменения обратимы и не изменяют последовательность ДНК, но они могут изменить то, как ваше тело читает последовательность ДНК. В биологии эпигенетика — это изучение наследственных изменений фенотипа, не связанных с изменениями в последовательности ДНК.
Тканевые стволовые клетки ощущают свое окружение, и это восприятие влияет на дальнейшую судьбу и функции. Стволовые клетки накапливают эпигенетические воспоминания о различных событиях окружающей среды. Стволовые клетки несут память об их первоначальной нише, миграции, столкновениях с воспалением и адаптации к новой судьбе и задачам.
www.science.org/doi/10.1126/science.abh2444
Анализ клонов отдельных стволовых клеток показал, что изменения метилирования при старении носят стохастический характер. Продолжительность жизни популяций МСК (мезенхимальных стволовых клеток) может сильно различаться из-за накопления (случайных) эпигенетических аберраций.
onlinelibrary.wiley.com/doi/full/10.1111/acel.12544
Дисфункция стволовых клеток – признак старения. Эпигенетические изменения играют решающую роль в потере функции стволовых клеток с возрастом.
Восстановление ядерного ацетил-КоА посредством эктопической экспрессии CiC или добавления ацетата к МСК в культуре омолаживает МСК, восстанавливая потенциал для эффективной дифференцировки по остеогенному клону. Цитрат, который, как недавно сообщалось, продлевает продолжительность жизни у дрозофилы, химически включает ацетил-КоА и может оказаться полезным для восстановления цитоплазматических и ядерных уровней ацетил-КоА. Следует установить общую применимость дефекта CiC к старым клеткам, особенно стволовым клеткам. Хроматиновое ремоделирование из-за деградации цитратов нарушает остеогенез выдержанных мезенхимальных стволовых клеток. doi.org/10.1038/s43587-021-00105-8
Старение сопровождается общим снижением функции многих клеточных путей. Старые мезенхимальные стволовые клетки демонстрируют пониженную доступность хроматина и более низкое ацетилирование гистонов, особенно на промоторах и энхансерах остеогенных генов. Снижение ацетил-я гистонов происходит из-за нарушения экспорта митохондриального ацетил-КоА из-за более низких уровней цитратного носителя (CiC). В старых клетках наблюдается усиленная лизосомная деградация CiC, которая опосредуется митохондриальнымими везикулами. Восстановление цитозольных уровней ацетил-КоА либо за счет экзогенной экспрессии CiC, либо за счет добавления ацетата, реконструирует ландшафт хроматина и устраняет дефекты остеогенеза старых МСК. Результаты показывают зависящую от возраста связь между контролем качества митохондрий, хроматином и судьбой СК, которые связаны между собой посредством CiC.
www.nature.com/articles/s43587-021-00105-8
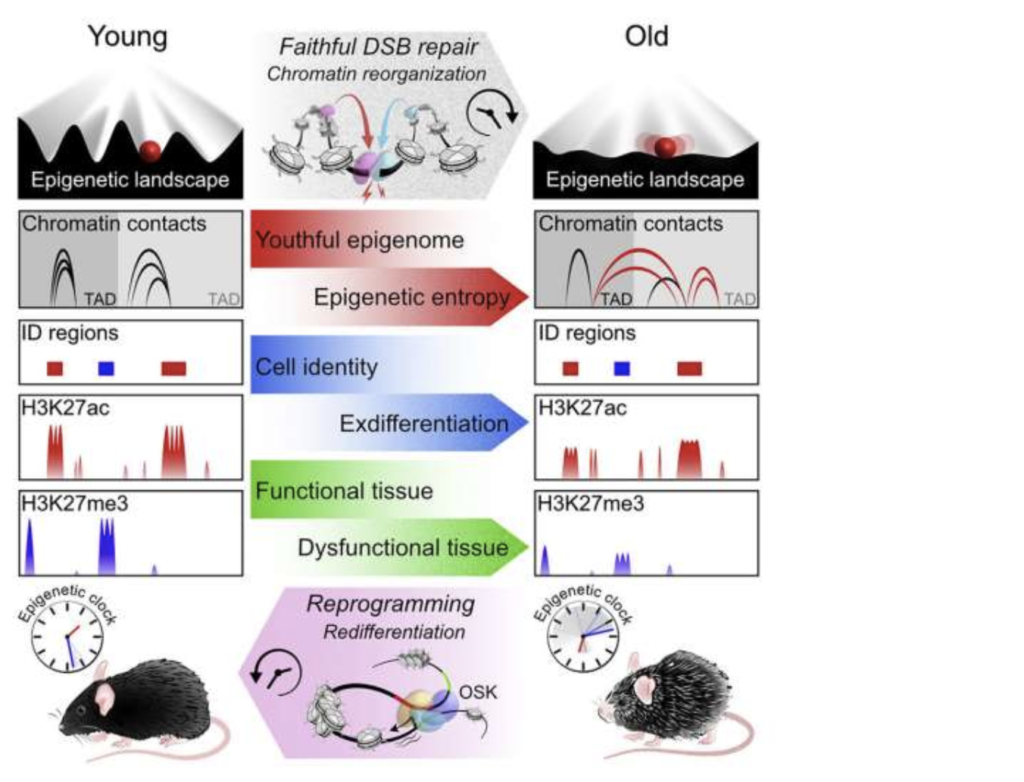
Исследование, которое проводилось 13 лет, демонстрирует, что деградация организации и регуляции ДНК, известная как эпигенетика, может вызывать старение организма независимо от изменений самого генетического кода. Нарушение эпигенетической информации приводит к старению мышей и что восстановление целостности эпигенома обращает вспять эти признаки старения. Это исследование является первым, которое показывает эпигенетические изменения как основную движущую силу старения у млекопитающих.
www.cell.com/cell/fulltext/S0092-8674(22)01570-7
Мы разрабатываем принципиально новые пути эпигенетического репрограммирования физическими методами.

